По какой формуле находится количество теплоты. Тема урока: "Количество теплоты
Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количествоv теплоты.
– это изменение внутренней энергии тела в процессе теплопередачи без совершения работы. Количество теплоты обозначают буквой Q .
Работа, внутренняя энергия и количество теплоты измеряются в одних и тех же единицах - джоулях (Дж ), как и всякий вид энергии.
В тепловых измерениях в качестве единицы количества теплоты раньше использовалась особая единица энергии - калория (кал ), равная количеству теплоты, необходимому для нагревания 1 грамма воды на 1 градус Цельсия (точнее, от 19,5 до 20,5 °С). Данную единицу, в частности, используют в настоящее время при расчетах потребления тепла (тепловой энергии) в многоквартирных домах. Опытным путем установлен механический эквивалент теплоты - соотношение между калорией и джоулем: 1 кал = 4,2 Дж .
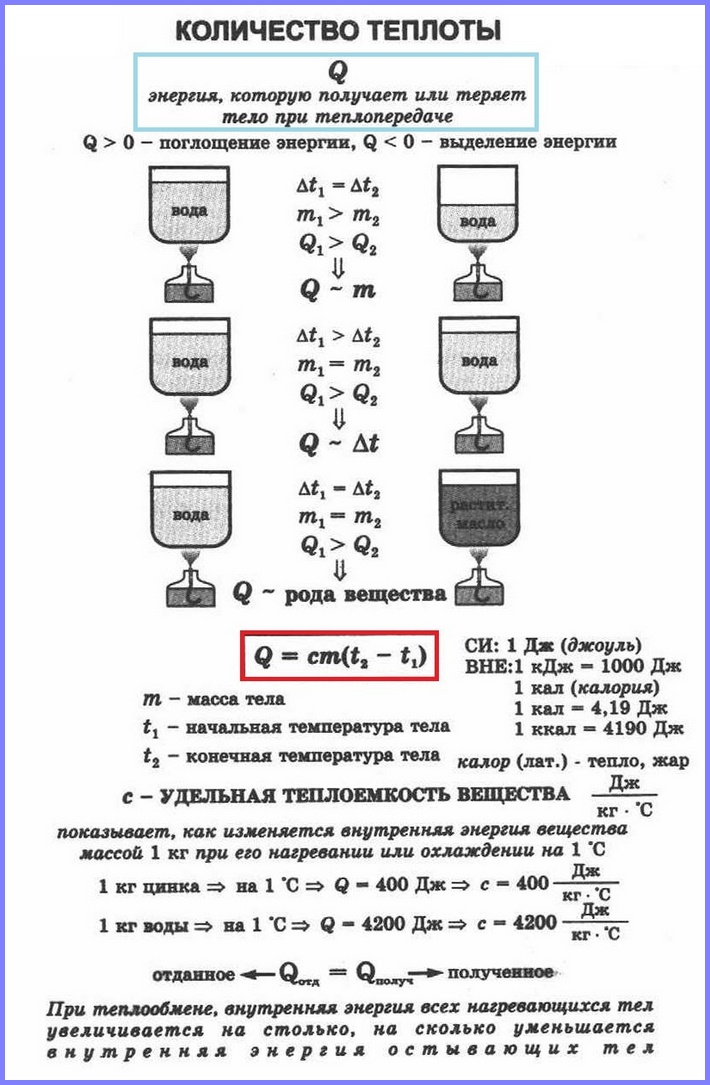
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество тепла требуется ему для нагревания. То же самое и с охлаждением.

Количество теплоты, необходимое для нагревания тела зависит еще и от рода вещества, из которого это тело сделано. Эта зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
– это физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К). Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой с . Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг °К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Поскольку кол-во теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С . В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Q , необходимое для нагревания тела массой m от температуры t 1 °С до температуры t 2 °С , равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.Q = c ∙ m (t 2 — t 1)
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.

Это конспект по теме «Количество теплоты. Удельная теплоёмкость» . Выберите дальнейшие действия:
- Перейти к следующему конспекту:
ТЕПЛООБМЕН.
1.Теплообмен.
Теплообмен или теплопередача – это процесс передачи внутренней энергии одного тела другому без совершения работы.
Существуют три вида теплообмена.
1) Теплопроводность – это теплообмен между телами при их непосредственном контакте.
2) Конвекция – это теплообмен, при котором перенос тепла осуществляется потоками газа или жидкости.
3) Излучение – это теплообмен посредством электромагнитного излучения.
2.Количество теплоты.
Количество теплоты – это мера изменения внутренней энергии тела при теплообмене. Обозначается буквой Q .
Единица измерения количества теплоты = 1 Дж.
Количество теплоты, полученное телом от другого тела в результате теплообмена, может тратиться на увеличение температуры (увеличение кинетической энергии молекул) или на изменение агрегатного состояния (увеличение потенциальной энергии).
3.Удельная теплоёмкость вещества.
Опыт показывает, что количество теплоты, необходимое для нагревания тела массой m от температуры Т 1 до температуры Т 2 пропорционально массе тела m и разности температур (Т 2 – Т 1), т.е.
Q = cm (Т 2 – Т 1 ) = с m Δ Т,
с называется удельной теплоёмкостью вещества нагреваемого тела.
![]()
Удельная теплоёмкость вещества равна количеству теплоту, которое необходимо сообщить 1 кг вещества, чтобы нагреть его на 1 К.
Единица измерения удельной теплоёмкости =.
Значения теплоёмкости различных веществ можно найти в физических таблицах.
Точно такое же количество теплоты Q будет выделяться при охлаждении тела на ΔТ.
4.Удельная теплота парообразования.
Опыт показывает, что количество теплоты, необходимое для превращения жидкости в пар, пропорционально массе жидкости, т.е.
Q = Lm ,
где коэффициент пропорциональности L называется удельной теплотой парообразования.
Удельная теплота парообразования равна количеству теплоты, которое необходимо для превращения в пар 1 кг жидкости, находящейся при температуре кипения.
Единица измерения удельной теплоты парообразования .
При обратном процессе, конденсации пара, теплота выделяется в том же количестве, которое затрачено на парообразование.
5.Удельная теплота плавления.
Опыт показывает, что количество теплоты, необходимое для превращения твёрдого тела в жидкость, пропорционально массе тела, т.е.
Q = λ m ,
где коэффициент пропорциональности λ называется удельной теплотой плавления.
Удельная теплота плавления равна количеству теплоты, которое необходимо для превращения в жидкость твёрдого тела массой 1 кг при температуре плавления.
Единица измерения удельной теплоты плавления .
При обратном процессе, кристаллизации жидкости, теплота выделяется в том же количестве, которое затрачено на плавление.
6.Удельная теплота сгорания.
Опыт показывает, что количество теплоты, выделяемое при полном сгорании топлива, пропорционально массе топлива, т.е.
Q = q m ,
Где коэффициент пропорциональности q называется удельной теплотой сгорания.
Удельная теплота сгорания равна количеству теплоты, которое выделяется при полном сгорании 1 кг топлива.
Единица измерения удельной теплоты сгорания.
7.Уравнение теплового баланса.
В теплообмене участвуют два или более тела. Одни тела отдают теплоту, а другие принимают. Теплообмен происходит до тех пор, пока температуры тел не станут равными. По закону сохранения энергии, количество теплоты, которое отдаётся, равно количеству, которое принимается. На этом основании записывается уравнение теплового баланса.
Рассмотрим пример.
Тело массой m 1 ,
теплоёмкость которого с 1 ,
имеет температуру Т 1 ,
а тело массой m 2 ,
теплоёмкость которого с 2 ,
имеет температуру Т 2 .
Причём Т 1
больше Т 2 .
Эти тела приведены в соприкосновение.
Опыт показывает, что холодное тело (m 2)
начинает нагреваться, а горячее тело
(m 1)
– охлаждаться. Это говорит о том, что
часть внутренней энергии горячего тела
передаётся холодному, и температуры
выравниваются. Обозначим конечную общую
температуру θ.
Количество теплоты, переданной горячим телом холодному
Q передан. = c 1 m 1 (Т 1 – θ )
Количество теплоты, полученной холодным телом от горячего
Q получен. = c 2 m 2 (θ – Т 2 )
По закону сохранения энергии Q передан. = Q получен. , т.е.
c 1 m 1 (Т 1 – θ )= c 2 m 2 (θ – Т 2 )
Раскроем скобки и выразим значение общей установившейся температуры θ.
![]()
Значение температуры θ в данном случае получим в кельвинах.
Однако, так как в выражениях для Q передан. и Q получен. стоит разность двух температур, а она и в кельвинах, и в градусах Цельсия одинакова, то расчёт можно вести и в градусах Цельсия. Тогда
![]()
В этом случае значение температуры θ получим в градусах Цельсия.
Выравнивание температур в результате теплопроводности можно объяснить на основании молекулярно-кинетической теории как обмен кинетической энергией между молекулами при сталкивании в процессе теплового хаотического движения.
Этот пример можно
проиллюстрировать графиком.
Наряду с механической энергией, любое тело (или система) обладает внутренней энергией. Внутренняя энергия – энергия покоя. Она складывается из теплового хаотического движения молекул, составляющих тело, потенциальной энергии их взаимного расположения, кинетической и потенциальной энергии электронов в атомах, нуклонов в ядрах и так далее.
В термодинамике важно знать не абсолютное значение внутренней энергии, а её изменение.
В термодинамических процессах изменяется только кинетическая энергия движущихся молекул (тепловой энергии недостаточно, чтобы изменить строение атома, а тем более ядра). Следовательно, фактически под внутренней энергией в термодинамике подразумевают энергию теплового хаотического движения молекул.
Внутренняя энергия U одного моля идеального газа равна:
Таким образом, внутренняя энергия зависит только от температуры. Внутренняя энергия U является функцией состояния системы, независимо от предыстории.
Понятно, что в общем случае термодинамическая система может обладать как внутренней, так и механической энергией, и разные системы могут обмениваться этими видами энергии.
Обмен механической энергией характеризуется совершенной работой А, а обмен внутренней энергией – количеством переданного тепла Q.
Например, зимой вы бросили в снег горячий камень. За счёт запаса потенциальной энергии совершена механическая работа по смятию снега, а за счёт запаса внутренней энергии снег был растоплен. Если же камень был холодный, т.е. температура камня равна температуре среды, то будет совершена только работа, но не будет обмена внутренней энергией.
Итак, работа и теплота не есть особые формы энергии. Нельзя говорить о запасе теплоты или работы. Это мера переданной другой системе механической или внутренней энергии. Вот о запасе этих энергий можно говорить. Кроме того, механическая энергия может переходить в тепловую энергию и обратно. Например, если стучать молотком по наковальне, то через некоторое время молоток и наковальня нагреются (это пример диссипации энергии).
Можно привести ещё массу примеров превращения одной формы энергии в другую.
Опыт показывает, что во всех случаях, превращение механической энергии в тепловую и обратно совершается всегда в строго эквивалентных количествах. В этом и состоит суть первого начала термодинамики, следующего из закона сохранения энергии.
Количество теплоты, сообщаемой телу, идёт на увеличение внутренней энергии и на совершение телом работы:
| , | (4.1.1) |
– это и есть первое начало термодинамики , или закон сохранения энергии в термодинамике.
Правило знаков: если тепло передаётся от окружающей среды данной системе, и если система производит работу над окружающими телами, при этом . Учитывая правило знаков, первое начало термодинамики можно записать в виде:
В этом выражении U – функция состояния системы; dU – её полный дифференциал, а δQ и δА таковыми не являются. В каждом состоянии система обладает определенным и только таким значением внутренней энергии, поэтому можно записать:
 , ,
|
Важно отметить, что теплота Q и работа А зависят от того, каким образом совершен переход из состояния 1 в состояние 2 (изохорически, адиабатически и т.д.), а внутренняя энергия U не зависит. При этом нельзя сказать, что система обладает определенным для данного состояния значением теплоты и работы.
Из формулы (4.1.2) следует, что количество теплоты выражается в тех же единицах, что работа и энергия, т.е. в джоулях (Дж).
Особое значение в термодинамике имеют круговые или циклические процессы, при которых система, пройдя ряд состояний, возвращается в исходное. На рисунке 4.1 изображен циклический процесс 1–а –2–б –1, при этом была совершена работа А.

Рис. 4.1
Так как U – функция состояния, то
| (4.1.3) |
Это справедливо для любой функции состояния.
Если то согласно первому началу термодинамики , т.е. нельзя построить периодически действующий двигатель, который совершал бы бóльшую работу, чем количество сообщенной ему извне энергии. Иными словами, вечный двигатель первого рода невозможен. Это одна из формулировок первого начала термодинамики.
Следует отметить, что первое начало термодинамики не указывает, в каком направлении идут процессы изменения состояния, что является одним из его недостатков.
>>Физика: Количество теплоты
Изменить внутреннюю энергию газа в цилиндре можно, не только совершая работу, но и нагревая газ.
Если закрепить поршень (рис.13.5
), то объем газа при нагревании не меняется и работа не совершается. Но температура газа, а следовательно, и его внутренняя энергия возрастают.
Процесс передачи энергии от одного тела к другому без совершения работы называют теплообменом
или теплопередачей.
Количественную меру изменения внутренней энергии при теплообмене называют количеством теплоты
. Количеством теплоты называют также энергию, которую тело отдает в процессе теплообмена.
Молекулярная картина теплообмена
При теплообмене не происходит превращения энергии из одной формы в другую, часть внутренней энергии горячего тела передается холодному телу.
Количество теплоты и теплоемкость.
Вам уже известно, что для нагревания тела массой m
от температуры t 1
до температуры t 2
необходимо передать ему количество теплоты:
При остывании тела его конечная температура t 2
оказывается меньше начальной температуры t 1
и количество теплоты, отдаваемое телом, отрицательно.
Коэффициент c
в формуле (13.5) называют удельной теплоемкостью
вещества. Удельная теплоемкость - это величина, численно равная количеству теплоты, которое получает или отдает вещество массой 1 кг при изменении его температуры на 1 К.
Удельная теплоемкость зависит не только от свойств вещества, но и от того, при каком процессе осуществляется теплопередача. Если нагревать газ при постоянном давлении, то он будет расширяться и совершать работу. Для нагревания газа на 1°С при постоянном давлении ему нужно передать большее количество теплоты, чем для нагревания его при постоянном объеме, когда газ будет только нагреваться.
Жидкие и твердые тела расширяются при нагревании незначительно. Их удельные теплоемкости при постоянном объеме и постоянном давлении мало различаются.
Удельная теплота парообразования.
Для превращения жидкости в пар в процессе кипения необходима передача ей определенного количества теплоты. Температура жидкости при кипении не меняется. Превращение жидкости в пар при постоянной температуре не ведет к увеличению кинетической энергии молекул, но сопровождается увеличением потенциальной энергии их взаимодействия. Ведь среднее расстояние между молекулами газа много больше, чем между молекулами жидкости.
Величину, численно равную количеству теплоты, необходимому для превращения при постоянной температуре жидкости массой 1 кг в пар, называют удельной теплотой парообразования
. Эту величину обозначают буквой r
и выражают в джоулях на килограмм (Дж/кг).
Очень велика удельная теплота парообразования воды: r H2O
=2,256 10 6 Дж/кг при температуре 100°С. У других жидкостей, например у спирта , эфира, ртути, керосина, удельная теплота парообразования меньше в 3-10 раз, чем у воды.
Для превращения жидкости массой m
в пар требуется количество теплоты, равное:
При конденсации пара происходит выделение такого же количества теплоты:
Величину, численно равную количеству теплоты, необходимому для превращения кристаллического вещества массой 1 кг при температуре плавления в жидкость, называют удельной теплотой плавления .
При кристаллизации вещества массой 1 кг выделяется точно такое же количество теплоты, какое поглощается при плавлении.
Удельная теплота плавления льда довольно велика: 3,34 10 5 Дж/кг. «Если бы лед не обладал большой теплотой плавления, - писал Р. Б л эк еще в XVIII в., - то тогда весной вся масса льда должна была бы растаять в несколько минут или секунд, так как теплота непрерывно передается льду из воздуха. Последствия этого были бы ужасны; ведь и при существующем положении возникают большие наводнения и сильные потоки воды при таянии больших масс льда или снега».
Для того чтобы расплавить кристаллическое тело массой m , необходимо количество теплоты, равное:
Количество теплоты, выделяемое при кристаллизации тела, равно:
Внутренняя энергия тела меняется при нагревании и охлаждении, при парообразовании и конденсации, при плавлении и кристаллизации. Во всех случаях телу передается или от него отнимается некоторое количество теплоты.
???
1. Что называют количеством теплоты
?
2. От чего зависит удельная теплоемкость вещества?
3. Что называют удельной теплотой парообразования?
4. Что называют удельной теплотой плавления?
5. В каких случаях количество теплоты положительная величина, а в каких случаях отрицательная?
Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс
Содержание урока конспект урока опорный каркас презентация урока акселеративные методы интерактивные технологии Практика задачи и упражнения самопроверка практикумы, тренинги, кейсы, квесты домашние задания дискуссионные вопросы риторические вопросы от учеников Иллюстрации аудио-, видеоклипы и мультимедиа фотографии, картинки графики, таблицы, схемы юмор, анекдоты, приколы, комиксы притчи, поговорки, кроссворды, цитаты Дополнения рефераты статьи фишки для любознательных шпаргалки учебники основные и дополнительные словарь терминов прочие Совершенствование учебников и уроков исправление ошибок в учебнике обновление фрагмента в учебнике элементы новаторства на уроке замена устаревших знаний новыми Только для учителей идеальные уроки календарный план на год методические рекомендации программы обсуждения Интегрированные урокиЕсли у вас есть исправления или предложения к данному уроку,
Как мы уже знаем, внутренняя энергия тела может изменяться как при совершении работы, так и при помощи теплопередачи (не совершая работу). Главное различие между работой и количеством теплоты заключается в том, что работа определяет процесс преобразования внутренней энергии системы, который сопровождается трансформацией энергии из одного вида в другой.
В том случае, если изменение внутренней энергии протекает с помощью теплопередачи , переход энергии из одного тела в другое осуществляется за счет теплопроводности , излучения, либо конвекции .
Энергия, которую тело теряет или получает во время теплопередачи, называется количеством теплоты.
При вычислении количества теплоты, необходимо знать, какие величины влияют на него.
От двух одинаковых горелок будем нагревать два сосуда. В одном сосуде 1 кг воды, в другом – 2 кг. Температура воды в двух сосудах изначально одинакова. Мы можем видеть, что за одно и тоже время вода в одном из сосудов нагревается быстрее, хотя оба сосуда получают равное количество теплоты.
Таким образом, делаем вывод: чем больше масса данного тела, тем большее количество теплоты следует затратить, для того чтобы понизить, или повысить его температуру на такое же количество градусов.
Когда тело остывает, оно отдает соседним предметам тем большее количество теплоты, чем больше его масса.
Мы все знаем, что если нужно нагреть полный чайник воды до температуры 50°C, мы затратим меньше времени на это действие, чем для нагревания чайника с тем же объемом воды, но только до 100 °C. В случае номер один воде будет отдано меньшее количество теплоты, нежели во втором.
Таким образом, количество теплоты, требуемое для нагревания, напрямую зависит от того, на сколько градусов сможет нагреться тело. Можно сделать вывод: количество теплоты напрямую зависит от разности температур тела.
Но возможно ли определить количество теплоты, требуемой не для нагревания воды, а какого-нибудь другого вещества, допустим, масла, свинца или железа.
 Наполним один сосуд водой, а другой наполним растительным маслом. Массы воды и масла равные. Оба сосуда будем равномерно подогревать на одинаковых горелках. Начнем опыт при равной начальной температуре растительного масла и воды. Через пять минут, измерив температуры нагревшихся масла и воды, мы заметим, что температура масла намного выше температуры воды, хотя обе жидкости получали одинаковое количество тепла.
Наполним один сосуд водой, а другой наполним растительным маслом. Массы воды и масла равные. Оба сосуда будем равномерно подогревать на одинаковых горелках. Начнем опыт при равной начальной температуре растительного масла и воды. Через пять минут, измерив температуры нагревшихся масла и воды, мы заметим, что температура масла намного выше температуры воды, хотя обе жидкости получали одинаковое количество тепла.
Напрашивается очевидный вывод: при нагревании равных масс масла и воды при одинаковой температуре нужно разное количество теплоты.
И мы тут же делаем еще одни вывод: количество теплоты, которое требуется для нагревания тела, напрямую зависит от вещества, из которого состоит само тело (рода вещества).
Таким образом, количество теплоты, нужное для нагревания тела (либо выделяемое при остывании), напрямую зависит от массы данного тела, вариативности его температуры, а также рода вещества.
Количество теплоты обозначают символом Q. Как и другие различные виды энергии, количество теплоты измеряется в джоулях (Дж) либо в килоджоулях (кДж).
1 кДж = 1000 Дж
Однако история показывает, что ученые стали измерять количество теплоты задолго того, как в физике появилось такое понятие как энергия. В то время, была выведена специальная единица для измерения количества теплоты – калория (кал) либо килокалория (ккал). Слово имеет латинские корни, калор – жара.
1 ккал = 1000 кал
Калория – это то количество теплоты, которое нужно для нагревания 1 г воды на 1°C
1 кал = 4,19 Дж ≈ 4,2 Дж
1 ккал = 4190 Дж ≈ 4200 Дж ≈ 4,2 кДж
Остались вопросы? Не знаете, как сделать домашнее задание?
Чтобы получить помощь репетитора – зарегистрируйтесь .
Первый урок – бесплатно!
сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
Предыдущая статья: Углерод — характеристика элемента и химические свойства Следующая статья: Чему равна скорость света
